Алкены и их химические свойства. Химические свойства алкенов
Простейшим алкеном является этен C 2 H 4 .По номенклатуре IUPAC названия алкенов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ен»; положение двойной связи указывается арабской цифрой.


Пространственная структура этилена
По названию первого представителя этого ряда - этилена - такие углеводороды называют этиленовыми.
Номенклатура и изомерия
Номенклатура
Алкены простого строения часто называют, заменяя суффикс -ан в алканах на -илен: этан - этилен, пропан - пропилен и т.д.
По систематической номенклатуре названия этиленовых углеводородов производят заменой суффикса -ан в соответствующих алканах на суффикс -ен (алкан - алкен, этан - этен, пропан - пропен и т.д.). Выбор главной цепи и порядок названия тот же, что и для алканов. Однако в состав цепи должна обязательно входить двойная связь. Нумерацию цепи начинают с того конца, к которому ближе расположена эта связь. Например:


Иногда используют и рациональные названия. В этом случае все алкеновые углеводороды рассматривают как замещенные этилена:

Непредельные (алкеновые) радикалы называют тривиальными названиями или по систематической номенклатуре:
Н 2 С = СН - - винил (этенил)
Н 2 С = CН - СН 2 - -аллил (пропенил-2)
Изомерия
Для алкенов характерны два вида структурной изомерии. Кроме изомерии, связанной со строением углеродного скелета (как у алканов), появляется изомерия, зависящая от положения двойной связи в цепи. Это приводит к увеличению числа изомеров в ряду алкенов.
Первые два члена гомологического ряда алкенов -(этилен и пропилен) - изомеров не имеют и их строение можно выразить так:
H 2 C = CH 2 этилен (этен)
H 2 C = CH - CH 3 пропилен (пропен)
Изомерия положения кратной связи
H 2 C = CH - CH 2 - CH 3 бутен-1
H 3 C - CH = CH - CH 3 бутен-2
Геометрическая изомерия - цис-, транс- изомерия.
Такая изомерия характерна для соединений с двойной связью.
Если простая σ -связь допускает свободное вращение отдельных звеньев углеродной цепи вокруг своей оси, то вокруг двойной связи такого вращения не происходит. Это и является причиной появления геометрических (цис-, транс- ) изомеров.
Геометрическая изомерия - один из видов пространственной изомерии.
Изомеры, у которых одинаковые заместители (при разных углеродных атомах) расположены по одну сторону от двойной связи, называют цис-изомерами,а по разную - транс-изомерами:


Цис- и транс- изомеры отличаются не только пространственным строением, но и многими физическими и химическими свойствами. Транс- изомеры более устойчивы, чем цис- изомеры.
Получение алкенов
В природе алкены встречаются редко. Обычно газообразные алкены (этилен, пропилен, бутилены) выделяют из газов нефтепереработки (при крекинге) или попутных газов, а также из газов коксования угля.
В промышленности алкены получают дегидрированием алканов в присутствии катализатора (Сr 2 О 3).
Дегидрирование алканов
H 3 C - CH 2 - CH 2 - CH 3 → H 2 C = CH - CH 2 - CH 3 + H 2 (бутен-1)
H 3 C - CH 2 - CH 2 - CH 3 → H 3 C - CH = CH - CH 3 + H 2 (бутен-2)
Из лабораторных способов получения можно отметить следующие:
1. Отщепление галогеноводорода от галогеналкилов при действии на них спиртового раствора щелочи:
2. Гидрирование ацетилена в присутствии катализатора (Pd):
H-C ≡ C-H + H 2 → H 2 C = CH 2
3. Дегидратация спиртов (отщепление воды).
В качестве катализатора используют кислоты (серную или фосфорную) или Аl 2 O 3:
В таких реакциях водород отщепляется от наименее гидрогенизированного (с наименьшим числом водородных атомов) углеродною атома (правило А.М.Зайцева):

Физические свойства
Физические свойства некоторых алкенов показаны в таблице ниже. Первые три представителя гомологического ряда алкенов (этилен, пропилен и бутилен) - газы, начиная с C 5 H 10 (амилен, или пентен-1) - жидкости, а с С 18 Н 36 - твердые вещества. С увеличением молекулярной массы повышаются температуры плавления и кипения. Алкены нормального строения кипят при более высокой температуре, чем их изомеры, имеющие изостроение. Температуры кипения цис -изомеров выше, чем транс -изомеров, а температуры плавления - наоборот.
Алкены плохо растворимы в воде (однако лучше, чем соответствующие алканы), но хорошо - в органических растворителях. Этилен и пропилен горят коптящим пламенем.
Физические свойства некоторых алкенов
Название |
t пл,°С |
t кип,°С |
||
Этилен (этен) |
||||
Пропилен (пропен) |
||||
Бутилен (бутен-1) |
||||
Цис-бутен-2 |
||||
Транс-бутен-2 |
||||
Изобутилен (2-метилпропен) |
||||
Амилен (пентен-1) |
||||
Гексилен (гексен-1) |
||||
Гептилен (гептен-1) |
||||
Октилен (октен-1) |
||||
Нонилен (нонен-1) |
||||
Децилен (децен-1) |
Алкены малополярны, но легко поляризуются.
Химические свойства
Алкены обладают значительной реакционной способностью. Их химические свойства определяются, главным образом, двойной углерод-углеродной связью.
π-Связь, как наименее прочная и более доступная, при действии реагента разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов, из которых состоит молекула реагента. Это можно представить в виде схемы:

Таким образом, при реакциях присоединения двойная связь разрывается как бы наполовину (с сохранением σ-связи).
Для алкенов, кроме присоединения, характерны еще реакции окисления и полимеризации.
Реакции присоединения
Чаще реакции присоединения идут по гетеролитическому типу, являясь реакциями электрофильного присоединения.
1. Гидрирование (присоединение водорода). Алкены, присоединяя водород в присутствии катализаторов (Pt, Pd, Ni), переходят в предельные углеводороды - алканы:
Н 2 С = СН 2 + H 2 → Н 3 С - СН 3 (этан)
2. Галогенирование (присоединение галогенов). Галогены легко присоединяются по месту разрыва двойной связи с образованием дигалогенопроизводных:
Н 2 С = СН 2 + Cl 2 → ClH 2 C - CH 2 Cl (1,2-дихлорэтан)
Легче идет присоединение хлора и брома, труднее - иода. Фтор с алкенами, как и с алканами, взаимодействует со взрывом.



Сравните: у алкенов реакция галогенирования - процесс присоединения, а не замещения (как у алканов).
Реакцию галогенирования обычно проводят в растворителе при обычной температуре.
Присоединение брома и хлора к алкенам происходит по ионному, а не по радикальному механизму. Этот вывод следует из того, что скорость присоединения галогена не зависит от облучения, присутствия кислорода и других реагентов, инициирующих или ингибирующих радикальные процессы. На основании большого числа экспериментальных данных для этой реакции был предложен механизм, включающий несколько последовательных стадий. На первой стадии происходит поляризация молекулы галогена под действием электронов π-связи. Атом галогена, приобретающий некоторый дробный положительный заряд, образует с электронами π-связи нестабильный интермедиат, называемый π-комплексом или комплексом с переносом заряда. Следует отметить, что в π-комплексе галоген не образует направленной связи с каким-нибудь конкретным атомом углерода; в этом комплексе просто реализуется донорно-акцепторное взаимодействие электронной пары π-связи как донора и галогена как акцептора.

Далее π-комплекс превращается в циклический бромониевый ион. В процессе образования этого циклического катиона происходит гетеролитический разрыв связи Br-Br и пустая р -орбиталь sp 2 -гибридизованного атома углерода перекрывается с р -орбиталью "неподеленной пары" электронов атома галогена, образуя циклический ион бромония.

На последней, третьей стадии анион брома как нуклеофильный агент атакует один из атомов углерода бромониевого иона. Нуклеофильная атака бромид-иона приводит к раскрытию трехчленного цикла и образованию вицинального дибромида (vic -рядом). Эту стадию формально можно рассматривать как нуклеофильное замещение S N 2 у атома углерода, где уходящей группой является Br + .

Результат этой реакции нетрудно предвидеть: анион брома атакует карбкатион с образованием дибромэтана.
Быстрое обесцвечивание раствора брома в СCl 4 служит одним из простейших тестов на ненасыщенность, поскольку и алкены, и алкины, и диены быстро реагируют с бромом.
Присоединение брома к алкенам (реакция бромирования) - качественная реакция на предельные углеводороды. При пропускании через бромную воду (раствор брома в воде) непредельных углеводородов желтая окраска исчезает (в случае предельных - сохраняется).
3. Гидрогалогенирование (присоединение галогеноводородов). Алкены легко присоединяют галогенводороды:
H 2 С = СН 2 + НВr → Н 3 С - CH 2 Вr
Присоединение галогенводородов к гомологам этилена идет по правилу В.В.Марковникова (1837 - 1904): при обычных условиях водород галогенводорода присоединяется по месту двойной связи к наиболее гидрогенизированному атому углерода, а галоген - к менее гидрогенизированному:

Правило Марковникова можно объяснить тем, что у несимметричных алкенов (например, в пропилене) электронная плотность распределена неравномерно. Под влиянием метильной группы, связанной непосредственно с двойной связью, происходит смещение электронной плотности в сторону этой связи (на крайний углеродный атом).
Вследствие такого смещения p-связь поляризуется и на углеродных атомах возникают частичные заряды. Легко представить, что положительно заряженный ион водорода (протон) присоединится к атому углерода (электрофильное присоединение), имеющему частичный отрицательный заряд, а анион брома - к углероду с частичным положительным зарядом.
Такое присоединение является следствием взаимного влияния атомов в органической молекуле. Как известно, электроотрицательность атома углерода немного выше, чем водорода.
Поэтому в метильной группе наблюдается некоторая поляризация σ-связей С-Н, связанная со смещением электронной плотности от водородных атомов к углероду. В свою очередь это вызывает повышение электронной плотности в области двойной связи и особенно на ее крайнем, атоме. Таким образом, метильная группа, как и другие алкильные группы, выступает в качестве донора электронов. Однако в присутствии пероксидных соединений или О 2 (когда реакция имеет радикальный характер) эта реакция может идти и против правила Марковникова.
По тем же причинам правило Марковникова соблюдается при присоединении к несимметричным алкенам не только галогеноводородов, но и других электрофильных реагентов (H 2 O, H 2 SО 4 , НОСl, ICl и др.).
4. Гидратация (присоединение воды). В присутствии катализаторов к алкенам присоединяется вода с образованием спиртов. Например:
H 3 C - CH = CH 2 + H - OH → H 3 C - CHOH - CH 3 (изопропиловый спирт)
Реакции окисления
Алкены окисляются легче, чем алканы. Продукты, образованные при окислении алкенов, и их строение зависят от строения алкенов и от условий проведения этой реакции.
1. Горение
Н 2 С = СН 2 + 3O 2 → 2СO 2 + 2Н 2 O
2. Неполное каталитическое окисление

3. Окисление при обычной температуре. При действии на этилен водного раствора КМnO 4 (при нормальных условиях, в нейтральной или щелочной среде - реакция Вагнера) происходит образование двухатомного спирта - этиленгликоля:
3H 2 C = CH 2 + 2KMnO 4 + 4H 2 O → 3HOCH 2 - CH 2 OH (этиленгликоль)+ 2MnO 2 + KOH
Эта реакция является качественной: фиолетовая окраска раствора перманганата калия изменяется при добавлении к нему непредельного соединения.
В более жестких условиях (окисление КМnO 4 в присутствии серной кислоты или хромовой смесью) в алкене происходит разрыв двойной связи с образованием кислородсодержащих продуктов:
H 3 C - CH = CH - CH 3 + 2O 2 → 2H 3 C - COOH (уксусная кислота)
Реакция изомеризации
При нагревании или в присутствии катализаторов алкены способны изомеризоваться - происходит перемещение двойной связи или установление изостроения.
Реакции полимеризации
За счет разрыва π-связей молекулы алкена могут соединяться друг с другом, образуя длинные цепные молекулы.

Нахождение в природе и физиологическая роль алкенов
В природе ациклические алкены практически не встречаются. Простейший представитель этого класса органических соединений - этилен C 2 H 4 - является гормоном для растений и в незначительном количестве в них синтезируется.
Один из немногих природных алкенов - мускалур (цис- трикозен-9) является половым аттрактантом самки домашней мухи (Musca domestica) .
Низшие алкены в высоких концентрациях обладают наркотическим эффектом. Высшие члены ряда также вызывают судороги и раздражение слизистых оболочек дыхательных путей
Отдельные представители
Этилен (этен) - органическое химическое соединение,описываемое формулой С 2 H 4 . Является простейшим алкеном. Содержит двойную связь и поэтому относится к ненасыщенным или непредельным углеводородам. Играет чрезвычайно важную роль в промышленности, а также является фитогормоном (низкомолекулярные органические вещества, вырабатываемые растениями и имеющие регуляторные функции).
Этилен - вызывает наркоз, обладает раздражающим и мутагенным действием.
Этилен - самое производимое органическое соединение в мире; общее мировое производство этилена в 2008 году составило 113 миллионов тонн и продолжает расти на 2-3% в год.
Этилен является ведущим продуктом основного органического синтеза и применяется для получения полиэтилена (1-е место, до 60 % всего объёма).
Полиэтилен - термопластичный полимер этилена. Самый распространенный в мире пластик.
Представляет собой воскообразную массу белого цвета (тонкие листы прозрачный бесцветны). Химически- и морозостоек, изолятор, не чувствителен к удару (амортизатор), при нагревании размягчается (80-120°С), при охлаждении застывает, адгезия (сцепление поверхностей разнородных твёрдых и/или жидких тел) - чрезвычайно низкая. Иногда в народном сознании отождествляется с целлофаном - похожим материалом растительного происхождения.
Пропилен - вызывает наркоз (сильнее, чем этилен), оказывает общетоксическое и мутагенное действие.
Устойчив к действию воды, не реагирует с щелочами любой концентрации, с растворами нейтральных, кислых и основных солей, органическими и неорганическими кислотами, даже концентрированной серной кислоты, но разлагается при действии 50%-ой азотной кислоты при комнатной температуре и под воздействием жидкого и газообразного хлора и фтора. Со временем, происходит термостарение.
Полиэтиленовая плёнка (особенно упаковочных, например, пузырчатая упаковка или скотч).


Тара (бутылки, банки, ящики, канистры, садовые лейки, горшки для рассады.
Полимерные трубы для канализации, дренажа, водо-, газоснабжения.

Электроизоляционный материал.
Полиэтиленовый порошок используется как термоклей.

Бутен-2 - вызывает наркоз, обладает раздражающим действием.
4.3.б. Присоединение галогеноводородов (гидрогалогенирование)
Другой важной реакций электрофильного присоединения к алкенам является давно известное гадрогалогенирование алкенов.
Ниже приведены типичные примеры присоединения HCl, HBr и HI к различным алкенам.


Влияние алкильных заместителей у двойной связи на скорость присоединения описывается следующей последовательностью:
R 2 C=CHR > RCH=CHR > RCH=CH 2
Это согласуется с таким механизмом, в котором в определяющей скорость стадии реакции происходит образование карбокатиона, поскольку стабильность алкильных катионов убывает в ряду третичный > вторичный > первичный. Таким образом, механизм присоединения должен включать промежуточное образование или свободного карбокатиона, что наблюдается редко, или интермедиата с карбокатионным характером. Последний случай наиболее типичен.
Если бы присоединение происходило через "свободный карбокатион", то реакция была бы совершенно нестереоселективной, так, как алкильные катионы имеют плоское строение. Однако, гидрогалогенирование, как правило, протекает стереоселективно, причем в зависимости от типа алкена может наблюдаться селективное анти -присоединение, селективное син - или смешанное син -анти -присоединение.
Для алкенов, у которых двойная связь не сопряжена с ароматическим кольцом, характерно анти -присоединение галогеноводорода. Анти -присоединение хлористого и бромистого водорода, хлористого и бромистого дейтерия наблюдается для циклогексена, циклопентена, 1,2-диметилгексена, 1,2-диметилпентена, цис - и транс -бутена-2, гексена-3 и многих других простых алкенов и циклоалкенов.
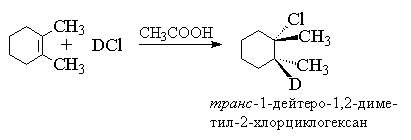
В продукте присоединения одинаковые заместители (метильные группы) расположены по разные стороны средней плоскости циклогексанового кольца, следовательно он относится к транс -ряду. Анти -присоединение трудно совместимо с механизмом, в котором предполагается образование дискретного карбокатиона. Для плоского карбокатиона нуклеофильная атака галогенид-иона равновероятна с обеих сторон плоскости, что должно привести к образованию смеси продуктов син - и анти -присоединения. Кинетика гидрогалогенирования алкенов также указывает на более сложный механизм присоединения. Для несопряженных алкенов скорость реакции описывается уравнением третьего порядка со вторым порядком по галогеноводороду, т. е. соответствует Ad E 3-механизму.
v = k [алкен] 2
Анти-присоединение и второй порядок реакции по галогеноводороду хорошо согласуется с Ad E 3-механизмом, в котором алкен взаимодействует с двумя молекулами галогеноводорода, одна из которых выполняет функцию электрофильного, а другая - нуклеофильного агента.

Такой тримолекулярный механизм предполагает, что первоначально образуется комплекс алкена и одной молекулой галогеноводорода с последующей атакой второй молекулы НХ на этот комплекс с анти -стороны без образования дискретного карбокатиона. Следует особо отметить, что любой тримолекулярный механизм должен состоять из двух последовательных стадий, поскольку одновременно столкновение трех молекул крайне маловероятно.

Анти-присоединение свидетельствует о предпочтительной нуклеофильной атаке галогеноводорода со стороны противоположной той, откуда происходит протонирование алкена. Вместо галогеноводорода функцию нуклеофильного агента в конечной стадии может выполнить и галогенид-ион. Действительно, скорость реакции обычно возрастает прямо пропорционально концентрации галогенид-иона, введенного в реакционную смесь в виде галогенидов тетраалкиламмония NR 4+ X - или лития LiX. В этом случае наблюдается стереоспецифическое анти -присоединение.
Для алканов, у которых двойная связь сопряжена с ароматическим кольцом, характерно син -присоединение или смешанное син -анти -присоединение галогеноводорода, например:

Син-присоединение является доминирующим процессом для цис - и транс -изомеров 1-фенилпропена, 1-фенил-4-алкилциклогексенов, аценафтилена, индена. При протонировании таких алкенов образуются карбокатионы бензильного типа, которые стабильнее чисто алкильных катионов, возникающих при протонировании обычных алкенов и циклоалкенов. Кинетика реакции в этом случае обычно описывается более простым уравнением второго порядка v = k[алкен], т. е. соответствует бимолекулярному Ad E 2-механизму. Ad E 2-Механизм предполагает образование ионной пары, включающей карбокатион и галогенид-ион.

Нельзя ожидать, что механизм присоединения с участием ионных пар будет отличаться высокой стереоселективностью. Если ионная пара превращается в конечный продукт быстрее, чем происходит вращение вокруг простой углерод-углеродной связи, конечным результатом будет син -присоединение, где протон и галогенид-ион присоединяется с одной и той же стороны двойной связи. В противном случае наблюдается образование продуктов как син - так и анти -присоединения НХ. Такой случай реализуется при гидрогалогенировании пара -замещенных стиролов Z-C 6 H 4 -CH=CH 2 . Наблюдаемая здесь закономерность заключается в том, что син -присоединение характерно лишь для тех олефинов, которые при протонировании дают относительно стабильный карбокатион, т. е. в случае донорных заместителей Z.
Для реакций гидрогалогенирования, протекающих по Ad E 2-механизму характерна конкуренция процессов сопряженного присоединения и перегруппировок, поскольку в качестве интермедиата образуется карбокатион или ионная пара.

В качестве примера перегруппировок с 1,2-миграцией алкильной группы и гидрид-иона приведем реакции гидрогалогенирования соответственно трет-бутилэтилена и изопропилэтилена.

При проведении этой же реакции без растворителя на холоду (-78 0 С) образуется смесь 33% нормального и 67% аномального (перегруппированного) продуктов присоединения.

4.3.в. Ориентация. Правило Марковникова
В отличие от симметричных электрофилов (Hal 2), галогеноводороды представляют собой несимметричные электрофильные реагенты. Присоединение любого несимметричного электрофила (HBr, ICl, H 2 O, Hg(OAc) 2 и т. д.) к несимметричному алкену в принципе могло бы дать смесь двух альтернативных продуктов, однако на практике обычно образуется только один из них. В качестве примера рассмотрим присоединение бромистого водорода к пропилену.

Еще в 1870 г. В.В. Марковников сформулировал эмпирическое правило, согласно которому несимметричные алкены присоединяют НХ таким путем, что преимущественно образуется продукт, в котором водород присоединяется к наименее замещенному, а Х - к наиболее замещенному концу двойной связи.
Обычно правило Марковникова объясняют различием в стабильности двух альтернативных карбокатионов. Например, в приведенном выше примере нормальный н -пропильный катион значительно менее стабилен, чем изопропильный катион, и поэтому реакция идет по второму пути.
Правило Марковникова первоначально использовалось только для случаев присоединения НХ к углеводородным субстратам, но в принципе его можно распространить и на реакции других замещенных алкенов. Так, присоединение НCl к CF 3 CH=CH 2 дает "анти -марковниковский" продукт CF 3 CH 2 CH 2 Cl. Этого и следовало ожидать, поскольку катион CF 3 CH+ CH 3 менее стабилен, чем катион CF 3 CH 2 CH 2+ из-за сильного (-I)-эффекта CF 3 -группы. Преимущественно образуется катион CF 3 CH 2 CH 2+ , но он тоже, хотя и в меньшей степени дестабилизирован индуктивным эффектом CF 3 -группы, вследствие чего присоединение HCl к трифторметилэтилену идет значительно медленнее, чем присоединение к незамещенному этилену.
По аналогичной причине катионы винилтриалкиламмония присоединяют HBr также против правила Марковникова:
Присоединение НХ к алкенам, имеющим сильные (-I) и (-M)-заместители, например, к акрилонитрилу или нитроэтилену также должно идти против правила Марковникова. Однако в этом случае двойная связь настолько сильно дезактивирована по отношению к электрофильным реагентам, что эти реакции идут лишь в очень жестких условиях. Хлористый винил СН 2 =СНСl всегда дает исключительно "марковниковские аддукты". Например, при его реакции с HCl образуется только 1,1-дихлорэтан (геминальный дихлорид) CH 3 CHCl 2 . Хлор, аналогично CF 3 -группе имеет сильный (-I)-эффект, и на первый взгляд, кажется, что по этой причине присоединение должно иметь антимарковниковскую ориентацию, т. к. катион + CH 2 CH 2 Cl должен быть более стабильным, чем катион СН 3 СН + Cl. Однако, в отличие от CF 3 -группы, хлор кроме (-I)-эффекта обладает также противодействующим ему (+М)-эффектом (т. к. имеет неподеленные пары). Опыт показывает, что величина мезомерного эффекта вполне достаточна, чтобы понизить энергию 1-хлорэтильного катиона ниже уровня энергии 2-хлорэтильного катиона, в котором +М-эффект не проявляется.
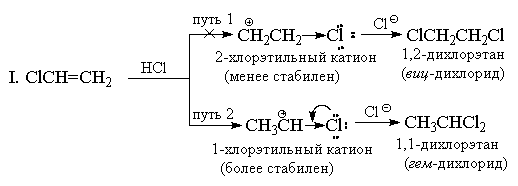
II. С позиций теории резонанса строение 1-хлорэтильного катиона может быть представлено следующим образом:
Тем не менее, присоединение к хлористому винилу происходит медленнее, чем к этилену в тех же условиях, т. е. по суммарному эффекту (-I > +M) хлор остается электроноакцепторным заместителем по сравнению с водородом, а 1-хлорэтильный катион менее стабилен, чем С 2 Н 5 + . Аналогичным образом реагируют с НХ и другие винилгалогениды.
Виниловые эфиры CH 2 =CHOR присоединяют НХ (X=Hal) по правилу Марковникова с гораздо большей скоростью, чем все перечисленные выше замещенные алкены. Это связано со значительным +М-эффектом RО-группы. В отличие от атома хлора, RО-группа по суммарному электронному эффекту (+М > -I) является сильным электронодонорным заместителем, эффективно стабилизирующим соседний карбокатионный центр. Строение карбокатиона в этом случае также может быть представлено в виде набора двух резонансных структур
Атака оксониевого катиона галогенид-анионом приводит к образованию -галогенэфиров типа СН 3 СН(Hal)OR.
4.3.г. Гидратация алкенов
Кислотно-катализируемая гидратация алкенов приводит к образованию спиртов. Направление гидратации алкенов определяется правилом Марковникова, поэтому предполагается, что в качестве промежуточной частицы в этой реакции образуется карбокатион.
Склонность вторичных алкильных карбокатионов к перегруппировкам мешает использованию гидратации алкенов для получения вторичных спиртов.

Этот метод в лаборатории нашел ограниченную область применения только для получения третичных спиртов. Реакция гидратации в этом случае в значительной степени обратима и третичные спирты образуются с низкими выходами (40-45%).
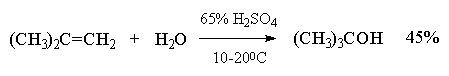

Гидратация простейших алкенов - этилена и пропилена - представляет собой важный промышленный метод получения этилового и изопропилового спиртов.

В лабораторной практике прямая гидратация алкенов не нашла широкого применения как вследствие жестких условий, так и благодаря образованию значительного количества изомерных спиртов. В настоящее время для региоселективного получения спиртов из алкенов обычно используется родственная реакция гидроксимеркурирования - демеркурирования.
4.3.д. Гидроксимеркурирование-демеркурирование
Электрофильная атака на двойную связь алкена может осуществляться ионами металлов, среди которых особое положение занимает катион ртути (II). Ацетат ртути в очень мягких условиях при 20 0 С присоединяется к алкенам в водном тетрагидрофуране (ТГФ) или в водной уксусной кислоте с образованием ртутьорганических соединений. Присоединение ацетата ртути по двойной связи протекает региоспецифично в строгом соответствии с правилом Марковникова, т. е. катион ртути присоединяется к наименее замещенному атому углерода.
Связь С-Hg в ртутьорганических соединениях может быть легко расщеплена под действием боргидрида натрия NaBH 4 , с образованием ртути и новой связи С-Н. Предполагается, что в качестве нестабильного интермедиата при этом получается алкилмеркургидрид, который далее разлагается с выделением металлической ртути по радикальному механизму.

Суммарно этот двухстадийный процесс гидроксимеркурирования-демеркурирования в конечном итоге представляет собой региоспецифичную гидратацию алкена по правилу Марковникова в исключительно мягких условиях, когда образование побочных продуктов сведено к предельно возможному минимуму. Это можно наглядно проиллюстрировать с помощью следующих примеров, в которых суммарный выход продуктов реакции составляет 90-98%. Приведенные цифровые данные в этом случае обозначают не выходы образующихся соединений, а их соотношение в смеси.
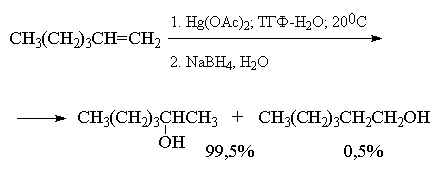



Как видно из приведенных выше примеров гидроксимеркурирование-демеркурирование алкенов в большинстве случаев обеспечивает региоспецифическую гидратацию алкенов с образованием практически только одного из двух изомерных спиртов. Следует отметить, что нет никакой необходимости в выделении ртутьорганического соединения, и оба процесса могут быть проведены непосредственно один за другим.
Гидроксимеркурирование несимметричных алкенов, по-видимому, начинается с атаки катиона AcOHg + и образования в качестве интермедиата несимметричного циклического меркуриниевого катиона (аналога несимметричного галогенониевого иона), который затем раскрывается в результате нуклеофильной атаки водой по наиболее замещенному атому углерода, несущему больший положительный заряд.

Мостиковый меркуриниевый ион можно зафиксировать в ненуклеофильной сильнокислой среде даже при 20 0 С при присоединении более сильного электрофильного агента - трифторацетата ртути в смеси фторсульфоновой кислоты и пятифтористой сурьмы.

Меркуриниевый катион может расщепляться не только при действии воды, но и других электронодонорных растворителей: спиртов, уксусной кислоты, ацетонитрила и др. Конечным продуктом реакции в этом случае будут соответственно простые эфиры, ацетаты или N-замещенные амиды уксусной кислоты, например:

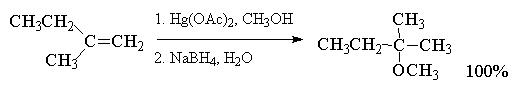
При использовании в реакции алкоксимеркурирования-демеркурирования разветвленных вторичных или третичных спиртов более эффективными, чем ацетат ртути, являются трифторацетат Hg(OCOCF 3) 2 или трифлат ртути Hg(OSO 2 CF 3) 2 .

Таким образом, гидрокси- и алкоксимеркурирование-демеркурирование - это один из лучших препаративных методов синтеза спиртов и простых эфиров с разветвленными алкильными радикалами.
Присоединение солей ртути к алкенам представляет собой наиболее яркий пример реакции сопряженного присоединения к двойной связи, где роль внешнего нуклеофильного агента выполняет растворитель. Стереохимия двойного процесса гидроксимеркурирования-демеркурирования зависит от стереохимического результата каждой отдельной стадии. Для гидроксимеркурирования характерно анти -присоединение, как и для других реакций с участием циклического катиона. Однако радикальное демеркурирование не отличается высокой стереоселективностью. Поэтому весь процесс в целом также нестереоспецифичен.
4.3.е. Присоединение алкенов (катионная димеризация и полимеризация алкенов)
Наиболее интересным примером такого типа реакций является димеризация и полимеризация изобутилена в присутствии серной кислоты.

Техническое название этой смеси алкенов - "диизобутилен". Данная реакция протекает по катионному механизму, сходному с механизмом присоединения минеральных кислот к двойной связи алкенов. На первой стадии протон присоединяется к молекуле изобутилена с образованием относительно стабильного трет -бутилкатиона. Далее образовавшийся трет -бутилкатион (кислота Льюиса) реагирует с молекулой изобутилена (основание Льюиса) с образованием нового стабильного третичного октильного катиона.
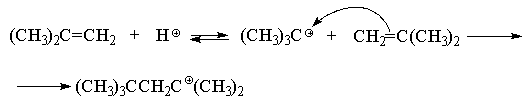
В данных условиях под действием оснований (H 2 O, HSO 4 - -ионы) октильный карбокатион быстро теряет протон и превращается в смесь изомерных пентенов, т. к. отрыв протона происходит из двух различных положений:

Преимущественное образование термодинамически менее стабильного алкена - 2,4,4-триметилпентена-1 (80% в реакционной смеси) связано с большей пространственной доступностью для атаки основанием атомов водорода метильных групп, по сравнению с атомами водорода метиленовой группы. В промышленности "диизобутилен" гидрируют на Ni-Ренея и получают "изооктан" (техническое название углеводорода 2,2,4-триметилпентана), используемый в качестве высокооктанового топлива для двигателей внутреннего сгорания.
При высоких концентрациях серной кислоты (более 80%) происходит катионная полимеризация изобутилена с образованием полимера, называемого полиизобутиленом (-CH 2 C(CH 3) 2 -) n . Этот каучукоподобный полимер используют для получения антикоррозионных и гидроизоляционных покрытий, герметиков и др.
Кроме изобутилена, по катионному механизму полимеризуются 3-метилбутен-1, виниловые эфиры и некоторые производные стирола, способные образовывать сравнительно устойчивые карбокатионы. В качестве катализаторов катионной полимеризации также используют фтористый водород и кислоты Льюиса: BF 3 , AlCl 3 , AlBr 3 и др. в присутствии очень малых количеств воды.
4.3.ж. Присоединение алканов (алкилирование алкенов)
Другой промышленный метод синтеза "изооктана" основан на взаимодействии изобутилена с избытком изобутана в присутствии концентрированной серной кислоты или в безводном фтористом водороде при 0 10 0 С.

Эта реакция также протекает по катионному механизму и, что особенно интересно, является примером цепного катионного процесса. Сначала изобутилен в условиях реакции димеризуется с образованием третичного октильного катиона (CH 3) 3 CCH 2 C + (CH 3) 2 . Подробно механизм его образования изложен в предыдущем разделе. Далее происходит быстрый перенос водорода (в виде гидрид-иона) от изобутана к октильному катиону с образованием молекулы "изооктана" и нового трет-бутилкатиона, который в свою очередь быстро реагирует с изобутиленом с образованием нового октильного катиона и т. д.
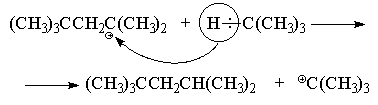
Кроме синтеза "изооктана", такой метод алкилирования используется в нефтехимической промышленности для синтеза высококипящих разветвленных углеводородов из разветвленных алкенов и алканов низкокипящих фракцией термического крекинга.
Химические свойства алканов
Алканами (парафинами) называют нециклические углеводороды, в молекулах которых все атомы углерода соединены только одинарными связями. Другими словами в молекулах алканов отсутствуют кратные — двойные или тройные связи. Фактически алканы являются углеводородами, содержащими максимально возможное количество атомов водорода, в связи с чем их называют предельным (насыщенными).
Ввиду насыщенности, алканы не могут вступать в реакции присоединения.
Поскольку атомы углерода и водорода имеют довольно близкие электроотрицательности, это приводит к тому, что связи С-Н в их молекулах крайне малополярны. В связи с этим для алканов более характерны реакции протекающие по механизму радикального замещения, обозначаемого символом S R .
1. Реакции замещения
В реакциях данного типа происходит разрыв связей углерод-водород
RH + XY → RX + HY
Галогенирование
Алканы реагируют с галогенами (хлором и бромом) под действием ультрафиолетового света или при сильном нагревании. При этом образуется смесь галогенпроизводных с различной степенью замещения атомов водорода — моно-, ди- три- и т.д. галогенозамещенных алканов.
На примере метана это выглядит следующим образом:
Меняя соотношение галоген/метан в реакционной смеси можно добиться того, что в составе продуктов будет преобладать какое-либо конкретное галогенпроизводное метана.
Механизм реакции
Разберем механизм реакции свободнорадикального замещения на примере взаимодействия метана и хлора. Он состоит из трех стадий:
- инициирование (или зарождение цепи) - процесс образования свободных радикалов под действии энергии извне – облучения УФ-светом или нагревания. На этой стадии молекула хлора претерпевает гомолитический разрыв связи Cl-Cl c образованием свободных радикалов:
Свободными радикалами, как можно видеть из рисунка выше, называют атомы или группы атомов с одним или несколькими неспаренными электронами (Сl , Н, СН 3 , СН 2 и т.д.);
2. Развитие цепи
Эта стадия заключается во взаимодействии активных свободных радикалов с неактивными молекулами. При этом образуются новые радикалы. В частности, при действии радикалов хлора на молекулы алкана, образуется алкильный радикал и хлороводород. В свою очередь, алкильный радикал, сталкиваясь с молекулами хлора, образует хлорпроизводное и новый радикал хлора:
3) Обрыв (гибель) цепи:
Происходит в результате рекомбинации двух радикалов друг с другом в неактивные молекулы:
2. Реакции окисления
В обычных условиях алканы инертны по отношению к таким сильным окислителям, как концентрированная серная и азотная кислоты, перманганат и дихромат калия (КMnО 4 , К 2 Cr 2 О 7).
Горение в кислороде
А) полное сгорание при избытке кислорода. Приводит к образованию углекислого газа и воды:
CH 4 + 2O 2 = CO 2 + 2H 2 O
Б) неполное сгорание при недостатке кислорода:
2CH 4 + 3O 2 = 2CO + 4H 2 O
CH 4 + O 2 = C + 2H 2 O
Каталитическое окисление кислородом
В результате нагревания алканов с кислородом (~200 о С) в присутствии катализаторов, из них может быть получено большое разнообразие органических продуктов: альдегиды, кетоны, спирты, карбоновые кислоты.
Например, метан, в зависимости природы катализатора, может быть окислен в метиловый спирт, формальдегид или муравьиную кислоту:
3. Термические превращения алканов
Крекинг
Крекинг (от англ. to crack — рвать) — это химический процесс протекающий при высокой температуре, в результате которого происходит разрыв углеродного скелета молекул алканов с образованием молекул алкенов и алканов с обладающих меньшими молекулярными массами по сравнению с исходными алканами. Например:
CH 3 -CH 2 -CH 2 -CH 2 -CH 2 -CH 2 -CH 3 → CH 3 -CH 2 -CH 2 -CH 3 + CH 3 -CH=CH 2
Крекинг бывает термический и каталитический. Для осуществления каталитического крекинга, благодаря использованию катализаторов, используют заметно меньшие температуры по сравнению с термическим крекингом.
Дегидрирование
Отщепление водорода происходит в результате разрыва связей С-Н; осуществляется в присутствии катализаторов при повышенных температурах. При дегидрировании метана образуется ацетилен:
2CH 4 → C 2 H 2 + 3H 2
Нагревание метана до 1200 °С приводит к его разложению на простые вещества:
СН 4 → С + 2Н 2
При дегидрировании остальных алканов образуются алкены:
C 2 H 6 → C 2 H 4 + H 2
При дегидрировании н -бутана образуются бутен-1 и бутен-2 (последний в виде цис- и транс -изомеров):
Дегидроциклизация
Изомеризация
Химические свойства циклоалканов
Химические свойства циклоалканов с числом атомов углерода в циклах больше четырех, в целом практически идентичны свойствам алканов. Для циклопропана и циклобутана, как ни странно, характерны реакции присоединения. Это обусловлено большим напряжением внутри цикла, которое приводит к тому, что данные циклы стремятся разорваться. Так циклопропан и циклобутан легко присоединяют бром, водород или хлороводород:
Химические свойства алкенов
1. Реакции присоединения
Поскольку двойная связь в молекулах алкенов состоит из одной прочной сигма- и одной слабой пи-связи, они являются довольно активными соединениями, которые легко вступаю в реакции присоединения. В такие реакции алкены часто вступают даже в мягких условиях — на холоду, в водных растворах и органических растворителях.
Гидрирование алкенов
Алкены способны присоединять водород в присутствии катализаторов (платина, палладий, никель):
CH 3 -СН=СН 2 + Н 2 → CH 3 -СН 2 -СН 3
Гидрирование алкенов легко протекает даже при обычном давлении и незначительном нагревании. Интересен тот факт, что для дегидрирования алканов до алкенов могут использоваться те же катализаторы, только процесс дегидрирования протекает при более высокой температуре и меньшем давлении.
Галогенирование
Алкены легко вступаю в реакцию присоединения с бромом как в водном растворе, так и с органических растворителях. В результате взаимодействия изначально желтые растворы брома теряют свою окраску, т.е. обесцвечиваются.
СН 2 =СН 2 + Br 2 → CH 2 Br-CH 2 Br
Гидрогалогенирование
Как нетрудно заметить, присоединение галогеноводорода к молекуле несимметричного алкена должно, теоретически, приводить к смеси двух изомеров. Например, при присоединении бромоводорода к пропену должны были бы получаться продукты:
Тем не менее в отсутствие специфических условий (например, наличие пероксидов в реакционной смеси) присоединение молекулы галогеноводорода будет происходить строго селективно в соответствии с правилом Марковникова:
Присоединении галогеноводорода к алкену происходит таким образом, что водород присоединяется к атому углерода с большим числом атомов водорода (более гидрированному), а галоген — к атому углерода с меньшим числом атомов водорода (менее гидрированному).
Гидратация
Данная реакция приводит к образованию спиртов, и также протекает в соответствии с правилом Марковникова:
Как легко догадаться, по причине того, что присоединение воды к молекуле алкена происходит согласно правилу Марковникова, образование первичного спирта возможно только в случае гидратации этилена:
CH 2 =CH 2 + H 2 O → CH 3 -CH 2 -OH
Именно по такой реакции проводят основное количество этилового спирта в крупнотоннажной промышленности.
Полимеризация
Специфическим случаем реакции присоединения можно реакцию полимеризации, которая в отличие от галогенирования, гидрогалогенирования и гадратации, протекает про свободно-радикальному механизму:
Реакции окисления
Как и все остальные углеводороды, алкены легко сгорают в кислороде с образованием углекислого газа и воды. Уравнение горения алкенов в избытке кислорода имеет вид:
C n H 2n + (3/2)nO 2 → nCO 2 + nH 2 O
В отличие от алканов алкены легко окисляются. При действии на алкены водного раствора KMnO 4 обесцвечивание, что является качественной реакцией на двойные и тройные CC связи в молекулах органических веществ.
Окисление алкенов перманганатом калия в нейтральном или слабощелочном растворе приводит к образованию диолов (двухатомных спиртов):
C 2 H 4 + 2KMnO 4 + 2H 2 O → CH 2 OH–CH 2 OH + 2MnO 2 + 2KOH (охлаждение)
В кислой среде происходит полное разрыв двойной связи с превращение атомов углерода образовывавших двойная связь в карбоксильные группы:
5CH 3 CH=CHCH 2 CH 3 + 8KMnO 4 + 12H 2 SO 4 → 5CH 3 COOH + 5C 2 H 5 COOH + 8MnSO 4 + 4K 2 SO 4 + 17H 2 O (нагревание)
В случае, если двойная С=С связь находится в конце молекулы алкена, то в качестве продукта окисления крайнего углеродного атома при двойной связи образуется углекислый газ. Связано это с тем, что промежуточный продукт окисления – муравьиная кислота легко сама окисляется в избытке окислителя:
5CH 3 CH=CH 2 + 10KMnO 4 + 15H 2 SO 4 → 5CH 3 COOH + 5CO 2 + 10MnSO 4 + 5K 2 SO 4 + 20H 2 O (нагревание)
При окислении алкенов, в которых атом C при двойной связи содержит два углеводородных заместителя, образуется кетон. Например, при окислении 2-метилбутена-2 образуется ацетон и уксусная кислота.
Окисление алкенов, при котором происходит разрыв углеродного скелета по двойной связи используется для установления их структуры.
Химические свойства алкадиенов
Реакции присоединения
Например, присоединение галогенов:
Бромная вода обесцвечивается.
В обычных условиях присоединение атомов галогена происходит по концам молекулы бутадиена-1,3, при этом π-связи разрываются, к крайним атомам углерода присоединяются атомы брома, а свободные валентности образуют новую π-связь. Таким образом, как бы происходит «перемещение» двойной связи. При избытке брома может быть присоединена еще одна его молекула по месту образовавшейся двойной связи.
Реакции полимеризации
Химические свойства алкинов
Алкины являются ненасыщенными (непредельными) углеводородами в связи с чем способны вступать в реакции присоединения. Среди реакци присоединения для алкинов наиболее распространено электрофильное присоединение.
Галогенирование
Поскольку тройная связь молекул алкинов состоит из одной более прочной сигма-связи и двух менее прочных пи-связей они способны присоединять как одну, так и две молекулы галогена. Присоединение одной молекулой алкина двух молекул галогена протекает по электрофильному механизму последовательно в две стадии:
Гидрогалогенирование
Присоединение молекул галогеноводорода, также протекает по электрофильному механизму и в две стадии. В обоих стадиях присоединение идет в соответствии с правилом Марковникова:
Гидратация
Присоединение воды к алкинами происходит в присутсвии солей рути в кислой среде и называется реакцией Кучерова.
В результате гидратации присоединения воды к ацетилену ообразуется ацетальдегид (укусный альдегид):
Для гомологов ацетилена присоединение воды приводит к образованию кетонов:
Гидрирование алкинов
Алкины реагируют с водородом в две ступени. В качестве катализаторов используют такие металлы как платина, палладий, никель:
Тримеризация алкинов
При пропускании ацетилена над активированным углем при высокой температуре из него образуется смесь различных продуктов, основным из которых является бензол – продукт тримеризации ацетилена:
Димеризация алкинов
Также ацетилен вступать в реакцию димеризации. Процесс протекает в присутствии солей меди как катализаторов:
Окисление алкинов
Алкины сгорают в кислороде:
С n H 2n-2 + (3n-1)/2 O 2 → nCO 2 + (n-1)H 2 O
Взаимодействие алкинов с основаниями
Алкины с тройной C≡C на конце молекулы, в отличие от остальных алкинов, способны вступать в реакции, в которых атом водорода при тройной связи замещается металл. Например, ацетилен реагирует с амидом натрия в жидком аммиаке:
HC≡CH + 2NaNH 2 → NaC≡CNa + 2NH 3 ,
а также с аммиачным раствором оксида серебра, образуя нерастворимые солеподобные вещества называемые ацетиленидами:
Благодаря такой реакции можно распознать алкины с концевой тройной связью, а также выделить такой алкин из смеси с другими алкинами.
Следует отметить, что все ацетилениды серебра и меди являются взрывоопасными веществами.
Ацетилениды способны реагировать с галогенпроизводными, что используется при синтезе более сложных органических соединений с тройной связью:
СН 3 -C≡CН + NaNН 2 → СН 3 -C≡CNa + NН 3
СН 3 -C≡CNa + CH 3 Br → СН 3 -C≡C-СН 3 + NaBr
Химические свойства ароматических углеводородов
Ароматический характер связи влияет на химические свойства бензолов и других ароматических углеводородов.
Единая 6пи–электронная система намного более устойчива, чем обычные пи-связи. Поэтому для ароматических углеводородов более характерны реакции замещения, а не присоединения. В реакции замещения арены вступают по электрофильному механизму.
Реакции замещения
Галогенирование
Нитрование
Лучше всего реакция нитрования протекает под действием не чистой азотной кислоты, а ее смеси с концентрированной серной кислотой, так называемой нитрующей смеси:
Алкилирование
Реакция при которой один из атомов водорода при ароматическом ядре замещается на углеводородный радикал:
Также вместо галогенпроизводных алканов можно использовать алкены. В качестве катализаторов можно использовать галогениды алюминия, трехвалентного железа или неорганические кислоты.<
Реакции присоединения
Гидрирование
Присоединение хлора
Протекает по радикальному механизму при интенсивном облучении ультрафиолетовым светом:
Подобным образом реакция может протекать только с хлором.
Реакции окисления
Горение
2С 6 Н 6 + 15О 2 = 12СО 2 + 6Н 2 О+Q
Неполное окисление
Бензольное кольцо устойчиво к действию таких окислителей как KMnO 4 и K 2 Cr 2 O 7 . Реакция не идет.
Деление заместителей в бензольном кольце на два типа:
Рассмотрим химические свойства гомологов бензола на примере толуола.
Химические свойства толуола
Галогенирование
Молекулу толуола можно рассматривать, как состоящую из фрагментов молекул бензола и метана. Поэтому логично предположить, что химические свойства толуола должны в какой-то мере сочетать химические свойства этих двух веществ, взятых по отдельности. В частyости, именно это и наблюдается при его галогенировании. Мы уже знаем, что бензол вступает в реакцию замещения с хлором по электрофильному механизму, и для осуществления данной реакции необходимо использовать катализаторы (галогениды алюминия или трехвалентного железа). В то же время метан так же способен реагировать с хлором, но уже по свободно-радикальному механизму, для чего требуется облучение исходной реакционной смеси УФ-светом. Толуол, в зависимости от того, в каких условиях подвергается хлорированию, способен дать либо продукты замещения атомов водорода в бензольном кольце – для это нужно использовать те же условия что и при хлорировании бензола, либо продукты замещения атомов водорода в метильном радикале, если на него, как и на метан действовать хлором при облучении ультрафиолетом:
Как можно заметить хлорирование толуола в присутствии хлорида алюминия привело к двум разным продуктам – орто- и пара-хлортолуолу. Это обусловлено тем, что метильный радикал является заместителем I рода.
Если хлорирование толуола в присутсвии AlCl 3 проводить в избытке хлора, возможно образование трихлорзамещенного толуола:
Аналогично при хлорировании толуола на свету при большем соотношении хлор/толуол можно получить дихлорметилбензол или трихлорметилбензол:
Нитрование
Замещение атомов водорода на нитрогрппу, при нитровании толуола смесью концентрированных азотной и серной кислот, приводит к продуктам замещения в ароматическом ядре, а не метильном радикале:
Алкилирование
Как уже было сказано метильный радикал, является ориентантом I рода, поэтому его алкилирование по Фриделю-Крафтсу приводит продуктам замещения в орто- и пара-положения:
Реакции присоединения
Толуол можно прогидрировать до метилциклогексана при использовании металлических катализаторов (Pt, Pd, Ni):
С 6 Н 5 СН 3 + 9O 2 → 7СO 2 + 4Н 2 O
Неполное окисление
При действии такого окислителя, как водный раствор перманганата калия окислению подвергается боковая цепь. Ароматическое ядро в таких условиях окислиться не может. При этом в зависимости от pH раствора будет образовываться либо карбоновая кислота, либо ее соль.
Алкены - непредельные углеводороды, в составе которых есть одна двойная связь. Примеры алкенов:

Методы получения алкенов.
1. Крекинг алканов при 400-700°С. Реакция идет по свободнорадикальному механизму:

2. Дегидрирование алканов:
3. Реакция элиминирования (отщепление): от соседних атомов углерода отщепляются 2 атома или 2 группы атомов, и образуется двойная связь. К таким реакциям относят:
А) Дегидратацию спиртов (нагрев свыше 150°С, при участии серной кислоты , как водоотнимающего реагента):
Б) Отщепление галогенводородов при воздействии спиртового раствора щелочи:

Атом водорода отщепляется преимущественно от того атома углерода, который связан с меньшим числом атомов водорода (наименее гидрогенизированного атома) - правило Зайцева .
В) Дегалогенирование:

Химические свойства алкенов.
Свойства алкенов обуславливаются наличием кратной связи, поэтому алкены вступают в реакции электрофильного присоединения, которое протекает в несколько стадий (Н-Х - реагент):
1-я стадия:

2-я стадия:
 .
.
Ион водорода в такого типа реакциях принадлежит тому атому углерода, который имеет более отрицательный заряд. Распределение плотности такое:

Если в качестве заместителя стоит донор, который проявляется +I- эффект, то электронная плотность смещается в сторону наиболее гидрогенизированного атома углерода, создавая на нем частично отрицательный заряд. Реакции идут по правилу Марковникова : при присоединении полярных молекул типа НХ (HCl , HCN , HOH и т.д.) к несимметричным алкенам водород присоединяется преимущественно к более гидрогенизированому атому углерода при двойной связи.
А) Реакции присоединения:
1) Гидрогалогенирование:
Реакция идет по правилу Марковникова. Но если в реакции присутствует пероксид , то правило не учитывается:
2) Гидратация. Реакция идет по правилу Марковникова в присутствие фосфорной или серной кислоты :

3) Галогенирование. В результате происходит обесцвечивание бромной воды - это качественная реакция на кратную связь:
4) Гидрирование. Реакция протекает в присутствие катализаторов.
Горят.
1. Горение на воздухе
2. Окисление водным раствором перманганата (реакция Вагнера)
В нейтральной среде получается коричневый оксид марганца (IV), а по двойной связи органического вещества присоединяются две ОН-группы:
Слева - алкен с перманганатом калия, справа - алкан. Органический слой (сверху) не смешивается с водным (снизу). Справа окраска перманганата не изменилась. Рис. 1.

Рис. 1. Реакция Вагнера
3. Окисление подкисленным раствором перманганата
В кислой среде раствор обесцвечивается: Мn +7 восстанавливается до Mn +2 . Обесцвечивание подкисленного раствора перманганата калия - качественная реакция на непредельные соединения .
5СН 2 =СН 2 + 12KMnO 4 + 18H 2 SO 4 = 12MnSO 4 + 10CO 2 + 6K 2 SO 4 + 28H 2 O.
Зависимость продуктов окисления от строения алкена:

Радикальное замещение в алкенах
Пропен и хлор при высокой температуре: 400-500 о С (условия, благоприятствующие радикальным реакциям) дают продукт не присоединения, а замещения.
В промышленности алкены получают крекингом или дегидрированием алканов нефти.
Лабораторные способы получения алкенов основаны на реакциях отщепления.
1. Дегалогенирование
Реакция дигалогеналканов, в молекулах которых атомы галогенов расположены у соседних атомов углерода, с магнием или цинком приводит к образованию двойной связи:
СН 2 Сl-CН 2 Сl + Zn → CH 2 =CH 2 + ZnCl 2
2. Дегидрогалогенирование
При взаимодействии галогеналканов с горячим спиртовым раствором щелочи отщепляется молекула галогеноводорода и образуется алкен:
СН 3 -СН 2 -СНCl-СН 3 + КОН спирт. CH 3 -CH=CH-CH 3 + KCl + H 2 O
3. Дегидратация
Нагревание спиртов с концентрированной серной или фосфорной кислотой приводит к отщеплению воды и образованию алкена.
Реакции отщепления несимметричных галогеналканов и спиртов часто протекают в соответствии с правилом Зайцева : Атом водорода преимущественно отщепляется от того из атомов С, который связан с наименьшим числом атомов Н.
Правило Зайцева, как и правило Марковникова, можно объяснить, сравнивая устойчивость промежуточных частиц, которые образуются в реакции.
Этилен, пропен и бутены - исходные вещества для нефтехимического синтеза, прежде всего для получения пластиков.
При присоединении хлора к алкенам получаются хлоропроизводные.
СН 2 =СН-СН 3 + Cl 2 → CH 2 Cl - CHCl - CH 3 (1,2-дихлорпропан)
Но еще в 1884 году русский ученый Львов М.Д. (рис. 2) провел реакцию хлорирования пропена в более жестких условиях, при t = 400 0 С. В результате получился продукт не присоединения хлора, а замещения.
СН 2 =СН-СН 3 + Cl 2 СН 2 =СН-СН 2 Cl + HCl

Рис. 2. Русский ученый М.Д. Львов
Взаимодействие одних и тех же веществ при разных условиях приводят к разным результатам. Эта реакция широко используется для получения глицерина. Иногда этилен используют в овощехранилищах для ускорения созревания плодов.
Подведение итога урока
На этом уроке вы рассмотрели тему «Алкены. Химические свойства - 2. Получение и применение алкенов». В ходе занятия вы смогли углубить свои знания об алкенах, узнали о химических свойствах алкенов, а также об особенностях получения и применения алкенов.
Список литературы
1. Рудзитис Г.Е. Химия. Основы общей химии. 10 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
2. Химия. 10 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2008. - 463 с.
3. Химия. 11 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2010. - 462 с.
4. Хомченко Г.П., Хомченко И.Г. Сборник задач по химии для поступающих в вузы. - 4-е изд. - М.: РИА «Новая волна»: Издатель Умеренков, 2012. - 278 с.
Домашнее задание
1. №№ 12, 13 (с. 39) Рудзитис Г.Е., Фельдман Ф.Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
2. Какая реакция является качественной на этилен и его гомологи?
3. Может ли при хлорировании пропена происходить не присоединение, а замещение? С чем это связано?
 Роскосмос объявляет открытый набор в отряд космонавтов Как выбирают космонавтов
Роскосмос объявляет открытый набор в отряд космонавтов Как выбирают космонавтов Ковалентные связи с участием атома углерода Радикал
Ковалентные связи с участием атома углерода Радикал Королева Марго (Маргарита де Валуа) - биография, фото, личная жизнь принцессы
Королева Марго (Маргарита де Валуа) - биография, фото, личная жизнь принцессы Сообщение об авторе агния барто
Сообщение об авторе агния барто Как называется профессия который знает много языков
Как называется профессия который знает много языков Геркулес (мультсериал) Фил из геркулеса что за животное
Геркулес (мультсериал) Фил из геркулеса что за животное Факторы внешней среды, воздействующие на организм в процессе его жизнедеятельности, роста и развития
Факторы внешней среды, воздействующие на организм в процессе его жизнедеятельности, роста и развития